
 Первый протез межпозвоночного диска одобрен экспертами FDA Комиссия независимых экспертов, дающая рекомендации Управлению по контролю за продуктами и лекарствами США (FDA), признала искусственный межпозвоночный диск Prestige, разработанный компанией Medtronic Inc, безопасным и эффективным устройством.
Имплантация искусственного межпозвоночного диска, лицензии на клиническое использование которого добивается Medtronic, может стать более предпочтительной альтернативой операции - артродезу (неподвижному соединению) позвонков, применяющейся сейчас при дегенеративных заболеваниях и травмах межпозвоночных дисков.
Несмотря на отсутствие данных долговременных клинических наблюдений, эксперты FDA единогласно одобрили положительный отзыв на устройство.
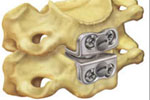
Протез межпозвоночного диска Prestige является первым устройством такого рода и предназначен для имплантации в шейный отдел, испытывающий наименьшую по сравнению с другими отделами позвоночника нагрузку. Диск изготовлен из нержавеющей стали и состоит из двух частей, соединенных подвижным соединением и крепящихся к соседним позвонкам при помощи шурупов. В отличие от артродеза позвонков, установка Prestige позволяет сохранить подвижность межпозвоночного соединения, что значительно повышает качество жизни пациентов.
Практически одновременно с Prestige Medtronic представила на рассмотрение FDA второй аналогичный протез – полиуритановый межпозвоночный диск со стальными креплениями под названием Brayan. Сегодняшнее решение экспертов FDA касалось исключительно диска Prestige.
Данные клинических испытаний Prestige, предоставленные Medntonic, охватывали сведения о пациентах в возрасте до 43 лет, наблюдение за которыми после установки протеза продолжалось в течение 12-24 месяцев. Однако, по словам экспертов и разработчиков, есть все основания полагать, что протез сможет сохранять функциональность на протяжении десятилетий.
По словам представителей Medtronic, лицензия на медицинское применение Prestige может быть выдана FDA в начале 2007 года.
По материалам МедНовости |

